Apakah Anda sedang mencari berapa mL larutan HNO2 0,1 M yang harus dicampurkan dengan 100 mL larutan NaNO2 0,1 M agar. Tentukan pH, jika iya? maka Anda berada di website yang tepat.
Semoga artikel berikut ini dapat bermanfaat.
Soal:
Berapa mL larutan HNO2 0,1 M yang harus dicampurkan dengan 100 mL larutan NaNO2 0,1 M agar diperoleh larutan dengan pH = 4 – log 2, jika diketahui Ka HNO2 = 4 × 10-4.
Pembahasan:
Dik:
Volume NaNO2 = 100 mL
[NaNO2] = 0,1 M
[HNO2] = 0,1 M
Ka HNO2 = 4 × 10-4
pH larutan = 4 – log 2, sehingga [H+] = 2 x 10-4
Dit: Volume HNO2 ?
Peny:
mol NaNO2 = 100 × 0,1 = 10 mmol
mol HNO2 = volume × [HNO2]
Campuran di atas merupakan larutan penyangga.
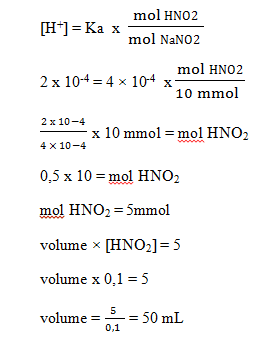
Jadi, volume HNO2 yang dicampurkan adalah sebanyak 50 mL.
Baca juga: Berapa gram CH3COONa (Mr = 82) yang harus dicampurkan dengan 100 mL larutan CH3COOH 0,1 M
Demikian yang dapat teknik area bagikan, tentang berapa mL larutan HNO2 0,1 M yang harus dicampurkan dengan 100 mL larutan NaNO2 0,1 M agar. Tentukan pH. Sekian dan terima kasih telah mengunjungi www.teknikarea.com, semoga bermanfaat dan sampai jumpa lagi di artikel kimia berikutnya.